【CMT&CHTV 文献精粹】
导读:本研究通过循环肿瘤DNA(ctDNA)检测进行的负向超选择可能是一种有效的策略,有助于识别那些最有可能从帕尼单抗治疗中受益的转移性结直肠癌(mCRC)患者。
结直肠癌(CRC)是全球常见的恶性肿瘤类型,mCRC的治疗选择对患者的生存率有着重要影响。在治疗mCRC的过程中,基因突变对于预测治疗效果和患者生存期起着关键作用。尽管已有研究揭示了KRAS、NRAS和BRAF等基因突变与抗表皮生长因子(EGFR)治疗抵抗性之间的关联,但如何更精准地预测治疗效果和患者生存期,仍是当前研究的重要挑战。此外,原发肿瘤的位置(左侧或右侧)对治疗决策的影响也日益受到研究者和临床医生的关注。
2024年3月,《Nature Medicine》杂志发表了一项题为《Baseline ctDNA gene alterations as a biomarker of survival after panitumumab and chemotherapy in metastatic colorectal cancer》的研究,重点研究了循环肿瘤DNA(ctDNA)基因变异作为预测mCRC患者在接受抗EGFR单克隆抗体Panitumumab和化疗后生存期的生物标志物的可能性,为上述问题提供了新的解决方案。
研究方法
本研究是一项预设性探索性生物标志物分析,旨在评估ctDNA基因突变与接受帕尼单抗(panitumumab)联合化疗的mCRC患者疗效结果之间的关联。研究包括了733名RAS野生型mCRC患者,他们提供了基线血浆样本以供ctDNA评估。研究使用了定制的基于下一代测序(NGS)的面板来检测与mCRC相关的基因突变、扩增和重排。
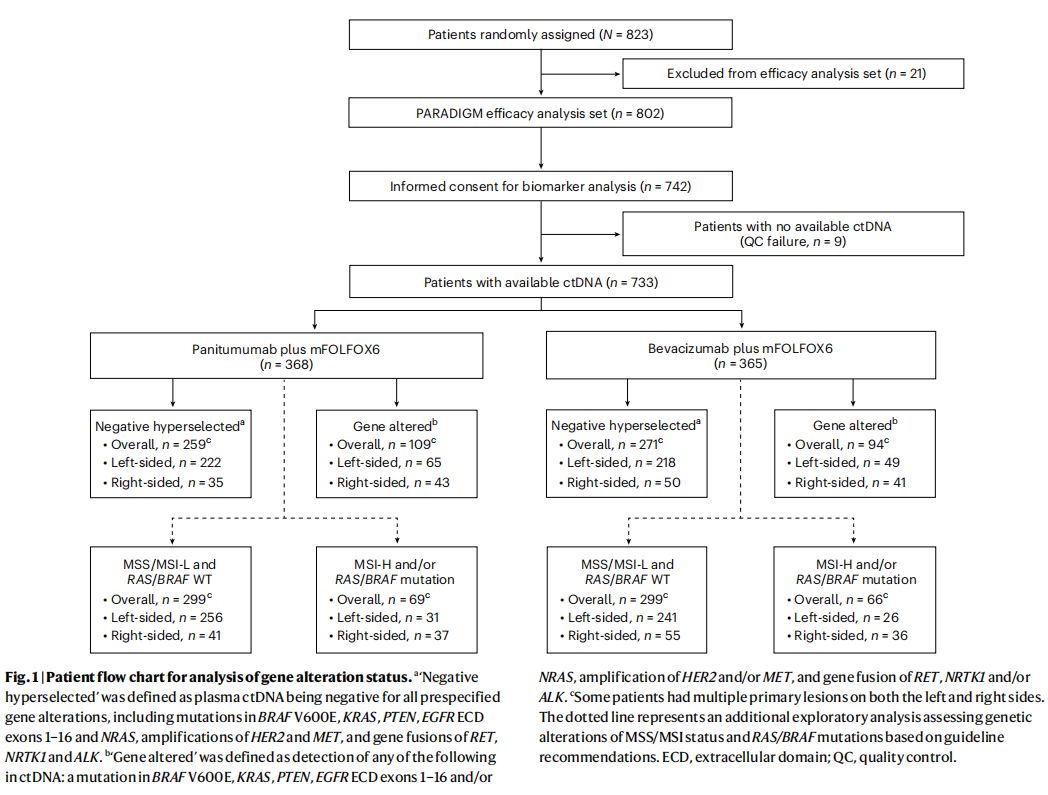
研究结果
ctDNA基因突变与OS和PFS的相关性结果显示,ctDNA基因突变状态与mCRC患者的总生存期(OS)密切相关。具体而言,ctDNA未检测到基因突变(即负向超选择)的患者,接受帕尼单抗联合mFOLFOX6治疗的中位OS为40.7个月,而接受贝伐珠单抗联合mFOLFOX6治疗的患者为34.4个月,风险比(HR)为0.76,表明帕尼单抗治疗组的生存期更长。
在无进展生存期(PFS)方面,负向超选择的患者在接受帕尼单抗治疗时,PFS与贝伐珠单抗治疗组相似。然而,在ctDNA检测到基因突变的患者中,帕尼单抗的PFS相较于贝伐珠单抗治疗组更短,这表明ctDNA基因突变状态可能是预测PFS的一个重要因素。
ctDNA基因突变与治疗响应率的相关性数据显示,在左侧原发性肿瘤的患者中,帕尼单抗联合mFOLFOX6治疗的响应率为83.3%,而贝伐珠单抗联合mFOLFOX6治疗的响应率为66.5%,这表明帕尼单抗治疗组的响应率显著更高(OR, 2.52; 95% CI, 1.61–3.98)。在右侧原发性肿瘤的患者中,尽管样本量较小,帕尼单抗治疗组的治疗响应率也表现出类似的趋势,为71.4%,而贝伐珠单抗治疗组为66.0%(OR, 1.29; 95% CI, 0.51–3.37)。
在整体负向超选择的患者群体中,帕尼单抗治疗的响应率为81.5%,贝伐珠单抗治疗的响应率为66.8%,帕尼单抗治疗组的响应率同样显著更高(OR, 2.19; 95% CI, 1.47–3.29)。
ctDNA基因突变与肿瘤位置和可切除率的相关性值得注意的是,研究中发现右侧结肠癌患者的ctDNA基因突变率较高,这与之前的研究结果一致。然而,即使是在右侧结肠癌患者中,负向超选择的患者也显示出较长的OS和PFS,以及改善的治疗响应率和肿瘤缩小深度。
结果显示,负向超选择的患者在接受帕尼单抗治疗时表现出更高的可切除率。在左侧原发性肿瘤的患者中,接受帕尼单抗治疗的患者的可切除率为19.8%,而接受贝伐珠单抗治疗的患者为10.6%,统计学差异显著(OR=2.10,95%CI 1.23–3.66)。在右侧原发性肿瘤的患者中,尽管样本量较小,帕尼单抗治疗组的可切除率也表现出类似的趋势,为14.3%,而贝伐珠单抗治疗组为14.0%。在整体负向超选择的患者群体中,帕尼单抗治疗的可切除率为18.9%,贝伐珠单抗治疗的可切除率为11.1%。

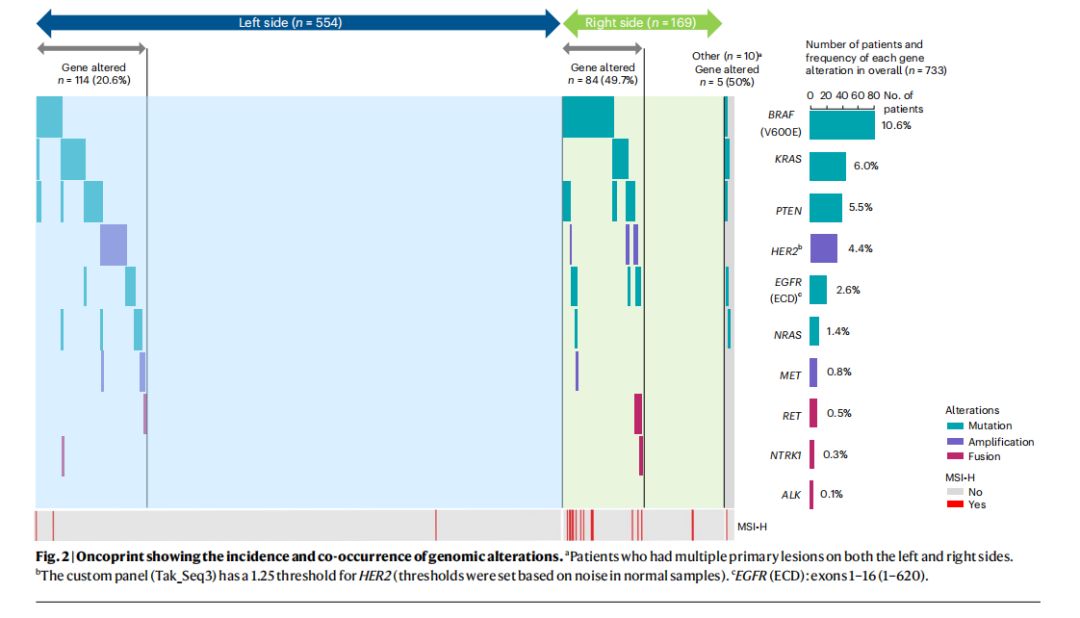


总结
上述结果表明,通过ctDNA检测进行的负向超选择可能是一种有效的策略,有助于识别那些最有可能从帕尼单抗治疗中受益的mCRC患者。此外,ctDNA检测为液体活检提供了一种微创且可能更全面的方法,用于识别与EGFR抑制剂抵抗性相关的基因变异。
这项研究提供了一种新的生物标志物检测方法,有助于个性化医疗的实施,使得治疗更加精准。ctDNA作为一种液体活检手段,为那些难以获取肿瘤组织样本的患者提供了另一种选择。此外,这项研究强调了ctDNA基因突变状态在预测抗EGFR治疗反应中的重要性,可能会改变临床实践中的治疗决策过程。未来的研究需要进一步验证这些发现,并探索ctDNA检测在mCRC治疗决策中的实际应用。
参考文献:Shitara K, Muro K, Watanabe J, et al. Baseline ctDNA gene alterations as a biomarker of survival after panitumumab and chemotherapy in metastatic colorectal cancer[J]. Nat Med. 2024 Mar;30(3):730-739.
编辑:十六
二审:清扬
三审:应泉
排版:半夏
封面图源:Pixabay
